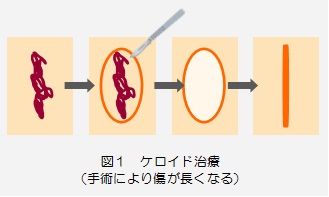
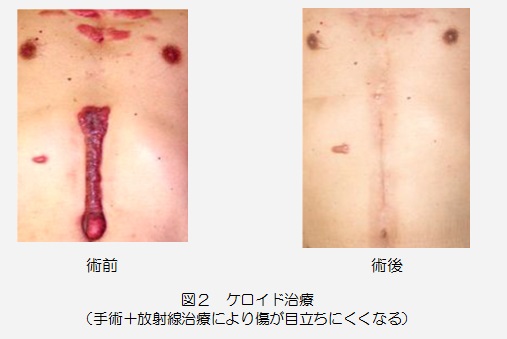
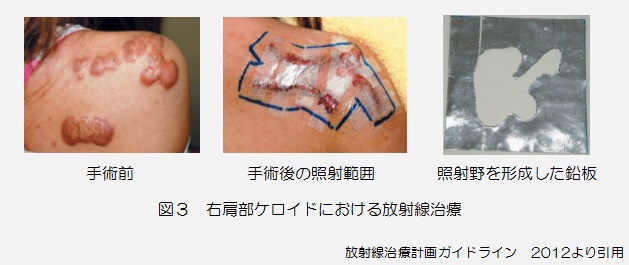
今回は、放射線治療における品質管理についてご紹介です。自施設での品質管理では無く、第三者機関による評価について書かせていただきます。
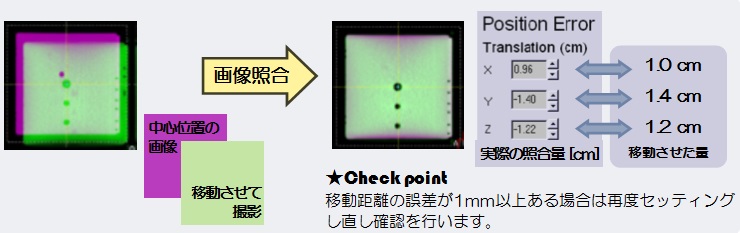
第三者の目でチェック
患者さんへ安全な医療を提供することは最も基本的な要件の一つであり、放射線治療においても、定期的な放射線治療装置の出力線量評価は必要不可欠なことであります。
2000年代初頭に国内の施設で判明した複数の誤照射事故の教訓から、施設内での安全管理体制のみならず、第三者機関による評価が必要と認識されるようになりました。そこで、2018年に「がん診療連携拠点病院の指定要件」において、第三者機関による出力線量測定を実施することが求められ、2021年には第三者機関による出力線量測定によって誤照射事故の存在が明らかになりました。
治療装置の出力線量が全国的に同一基準であることが放射線治療の基本ですので、施設の現状を知る上でも第三者機関による出力線量測定が重要な評価手段となっています。
実際の評価方法は?
第三者機関による出力線量測定は、訪問による調査と郵送による調査に分けられ、複数の機関や団体により実施されています。当院では、医療原子力技術研究振興財団1)の郵送による出力線量測定を受けています。郵送での評価は、IAEA(International Atomic Energy Agency)やWHO(World Health Organization)を始めとした機関により世界各国で実施されており、全世界の約60%の施設が郵送測定による第三者機関の評価を受けています。
出力線量測定の申し込み後、財団より出力線量測定セットが施設に送付されてきます。使用する線量計はガラス線量計2)で、決められた測定条件3)に基づき、ガラス線量計に照射を行います。照射後、出力線量測定セットを財団に返送し、財団の方で出力線量の読み取り・データを解析・評価をおこなう流れです。結果は2週間程で施設に届きます。
出力線量の評価は、基準線量に対し±5%以内を許容範囲とし、±5%を超える場合には、財団より施設の品質管理担当者へのヒアリングが行われ、測定手順等に相違はないか確認が行われます。その上で再測定の希望の有無が確認されます。基準線量の±10%を超える場合については、品質管理担当者へのヒアリング後、早急に施設の基準線量計で再測定の実施が求められ、必要に応じ訪問調査の有無が確認されます。当院での結果(右図)は、いずれも±1%未満でとても良い結果を得ることができました。この結果に甘んじることなく、日々品質管理に努めていかなければならないと思っております。
1)公益財団法人 医用原子力技術研究振興財団(ANTM : Association for Nuclear Technology in Medicine):平成8年3月に設立。各種放射線による疾病の治療・診断等、医用原子力技術の研究を推進し、普及を図ることにより科学技術の振興を図り、もって人類の福祉向上に寄与することを目的とする財団。
2)蛍光ガラス線量計:ラジオフォトルミネセンス(RPL : Radio photo luminescence)現象を利用した固体線量計。紫外線や読み取り操作等による消滅がなく、フェーディングの影響が極めて小さいなど優れた特性を持つ。繰り返し読み取り・使用が可能。
3)測定条件:測定エネルギーは任意(当院では、4・6・10MVのX線3本)。照射野サイズは、10cm×10cmの校正条件および任意のサイズ(当院では校正条件プラス5cm×5cm)。10cm深位置で、吸収線量が100cGyとなるMU値を治療計画装置で算出し照射。その他、任意条件での測定あり。
第三者機関による評価についは、3年に1回実施することが推奨されています。当院も今年がちょうど前回の実施から3年目となりますので、現在、評価に向けての準備をしております。
当院は地域に密着した放射線治療の提供を目指しております。これまで以上に地域の皆様へ安全で安心できる放射線治療を提供して参りますので、引き続きよろしくお願いいたします